近期,中南大學(xué)湘雅藥學(xué)院周文虎教授-謝努力副教授團(tuán)隊(duì)聯(lián)合湘雅醫(yī)院趙爽副研究員在國(guó)際權(quán)威期刊《Advanced Science》(中科院一區(qū)TOP期刊,影響因子14.3)以Research Article形式發(fā)表題為“Targeted DNA Nanomachine Enables Specific miRNA-Responsive Singlet Oxygen Amplification for Precise Cutaneous Squamous Cancer Therapy(特異性miRNA響應(yīng)的單線態(tài)氧放大的DNA納米機(jī)器用于皮膚鱗狀細(xì)胞癌的治療)”的原創(chuàng)性論文。

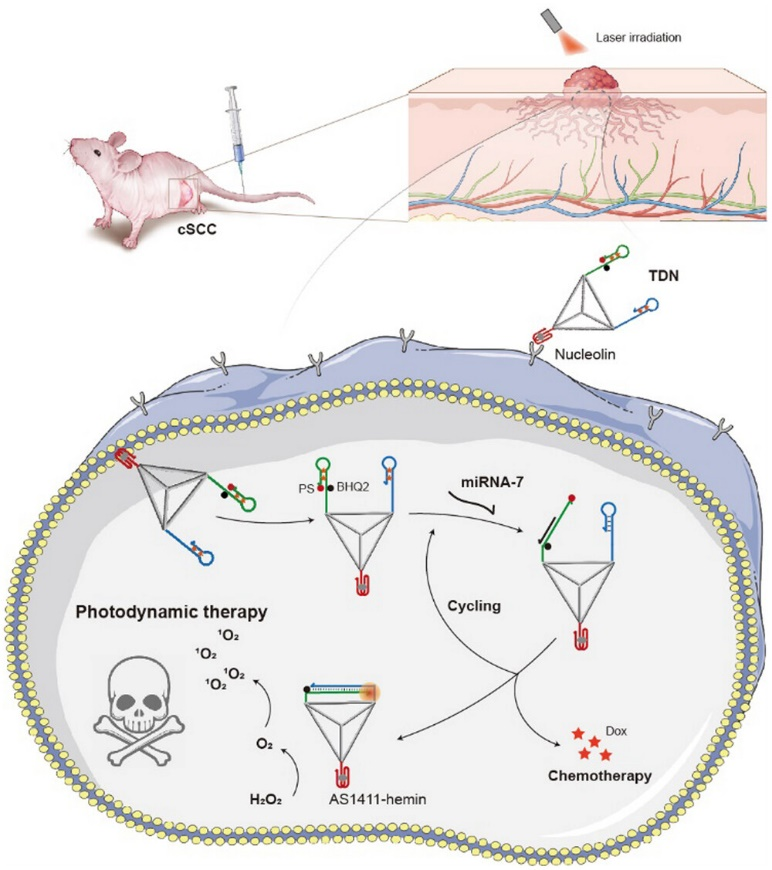
光動(dòng)力療法(PDT)是治療包括皮膚鱗狀細(xì)胞癌(cSCC)在內(nèi)的皮膚相關(guān)腫瘤的有效策略。但其臨床應(yīng)用仍面臨雙重挑戰(zhàn):如何在保證療效的同時(shí)降低光毒性脫靶風(fēng)險(xiǎn),以及如何克服腫瘤缺氧微環(huán)境對(duì)氧依賴性光敏劑的抑制作用。為解決上述問題,團(tuán)隊(duì)構(gòu)建了一種基于四面體DNA框架的智能納米系統(tǒng),通過整合腫瘤靶向適配體與miRNA響應(yīng)性發(fā)夾DNA催化組裝(HCA)模塊,實(shí)現(xiàn)了cSCC的精準(zhǔn)協(xié)同治療。該系統(tǒng)經(jīng)適配體靶向遞送后,由cSCC特異性miRNA激活HCA級(jí)聯(lián)反應(yīng),觸發(fā)光敏劑(PS)的原位擴(kuò)增與化療藥物的可控釋放。此外,通過將具有類過氧化氫酶活性的血紅素整合至DNA骨架,有效催化腫瘤微環(huán)境內(nèi)過氧化氫分解產(chǎn)氧,解決了腫瘤微環(huán)境缺氧問題。
經(jīng)體外實(shí)驗(yàn)及荷瘤小鼠模型證實(shí),該納米系統(tǒng)可顯著增強(qiáng)抗腫瘤效應(yīng),實(shí)現(xiàn)cSCC的高效消融,且未觀察到系統(tǒng)性毒副反應(yīng)及組織炎癥。本研究不僅為腫瘤特異性miRNA的診療應(yīng)用提供了新范式,也為皮膚腫瘤的無(wú)創(chuàng)精準(zhǔn)治療開辟了創(chuàng)新路徑。
該研究得到了國(guó)家自然科學(xué)基金和湖南省自然科學(xué)基金的支持。中南大學(xué)湘雅藥學(xué)院為該論文的第一通訊單位。中南大學(xué)湘雅藥學(xué)院博士研究生Hanane Aliouat和湘雅醫(yī)院博士研究生張德闐為本文共同第一作者,謝努力副教授、周文虎教授和趙爽副研究員為共同通訊作者。
原文連接:DOI:org/10.1002/advs.202415296
(一審:謝努力,二審:周文虎,三審:曹東升)